

Преимплантационная генетическая диагностика методом сравнительной геномной гибридизации — новый подход в профилактике рождения детей с врожденной и наследственной патологией в рамках программы ВРТ
Что такое преимплантационная генетическая диагностика (ПГД)?
Преимплантационная генетическая диагностика – это исследование эмбрионов на стадии доимплантационного развития, то есть пока эмбрион еще не перенесен в матку женщины и находится в инкубаторе в чашках для культивирования. На этой стадии развития имеется возможность провести генетическое исследование самих эмбрионов. Во всем мире данное исследование широко применяется в медицинской практике в программе ЭКО. Это связано с тем, что перенос заведомо здоровых эмбрионов повышает процент наступления беременности, снижает процент выкидышей, способствует рождению детей без генетической патологии в программе ЭКО и тем самым повышает эффективность лечения бесплодия. Исследователями разных стран доказано, что эмбрионы с неправильной генетикой зачастую останавливаются на разных стадиях своего развития: до имплантации, и на любом сроке беременности или при рождении дают пороки развития и умственную отсталость. Это происходит по причине сбоя в программе развития эмбриона, которая прописана в генах, т. е. эмбрион неправильно развивается. К сожалению эмбрионы с генетической патологией в программе ЭКО внешне не отличаются от эмбрионов без патологии и обычно врачи переносят в полость матки внешне морфологически «красивые» эмбрионы. Таким образом, при переносе генетически здоровых эмбрионов уменьшается количество попыток ЭКО (гормональная нагрузка на организм сводится к минимуму), а время достижения результата ЭКО, рождение здорового ребенка, сокращается.
Кому показана ПГД?
- Парам, у которых в анамнезе были случаи рождения детей с наследственной и врожденной патологией.
- парам, в кариотипе которых имеются сбалансированные хромосомные аберрации (транслокации и др).
ПГД у пациентов с нарушением в кариотипе является одним из главных звеньев в алгоритме профилактических мероприятий по предотвращению не только рождения больного ребенка в таких семьях, но и предотвращению у них возникновения беременности больным плодом. У этой группы пациентов помимо исследования эмбрионов на анеуплоидии хромосом, вовлеченных в транслокации, необходимо дополнительно исследовать их на самые распространенные хромосомные нарушения (синдромы Дауна, Патау, Эдвардса).
- парам, возраст которых превышает 35 лет.
Исследования показали четкую корреляцию возраста женщин с частотой хромосомной патологии у эмбрионов. Чем старше возраст женщин, тем большее количество их эмбрионов содержит генетическую патологию, зачастую по нескольким хромосомам одновременно.
- парам, в анамнезе которых было 2 и более неудачных попыток ЭКО.
Неудачные попытки ЭКО могут быть связаны с переносом эмбрионов с генетической патологией.
- парам, у которых в анамнезе были случаи пузырного заноса, неразвивающиеся беременности, невынашивание беременности;
Как в популяции, так и после программы ВРТ основное количество (75-80%) прерываний беременности приходится на I триместр. В основе невынашивания беременности у этого контингента лиц могут лежать как генетические отклонения эмбриона, так многоплодие. ПГД у пациентов с невынашиванием беременности может снизить частоту спонтанных выкидышей до общепопуляционных показателей. У пациентов с выкидышами в анамнезе уровень спонтанных абортов удалось снизить до 16.7% против ожидаемых 36.5%, у женщин старше 35 - до 12% против ожидаемых 44.5%.
- парам, где у мужчин в сперматозоидах отмечается высокий процент различной генетической патологией.
Изучение хромосом в сперматозоидах, полученных от мужчин с олиго, астено, тератозооспермией (ОАТ), включенных в программу ЭКО, выявило повышенный уровень анеуплоидии (неправильный набор хромосом) по сравнению с мужчинами без отклонений в показателях спермограммы. У мужчин с нормальным кариотипом показатель частоты анеуплоидии половых хромосом в сперматозоидах наблюдали при олигоастенотератозооспермии в 4 раза чаще, чем при нормальной спермограмме. Использование сперматозоидов с неправильным хромосомным набором для оплодотворения приведет к формированию эмбриона с генетической патологией, а это в свою очередь к неразвивающейся беременности или рождению больного ребенка. Было показано, что до 20% хромосомных нарушений, например, трисомия при болезни Дауна, являются следствием оплодотворения нормальной яйцеклетки патологическим сперматозоидом даже при нормальных показателях спермограммы.
- по желанию парам, которые хотят провести скрининг эмбрионов на генетическую патологию (анеуплоидии), быть уверенными в здоровье будущих детей и повысить эффективность лечения методами ВРТ.
У любой супружеской пары, даже если в семье не отмечены случаи рождения больного ребенка, к сожалению, все равно остается риск возникновения генетической патологии у плода. Зачастую мутации в потомстве возникают впервые. Эмбрионы, имеющие анеуплоидию, могут быть хорошего качества от 71% до 88.5%. С другой стороны, у пациентов с нарушением репродуктивной функции генетические нарушения отмечаются чаще. Проводя программу ВРТ, следует помнить, что ее цель – не только наступление беременности, но и рождение здоровых детей. В современных клиниках преимплантационная генетическая диагностика, в последнее время, стала необходимой составляющей при проведении экстракорпорального оплодотворения и направлена на выявление наследственных и врожденных заболеваний у эмбрионов до переноса в полость матки женщины.
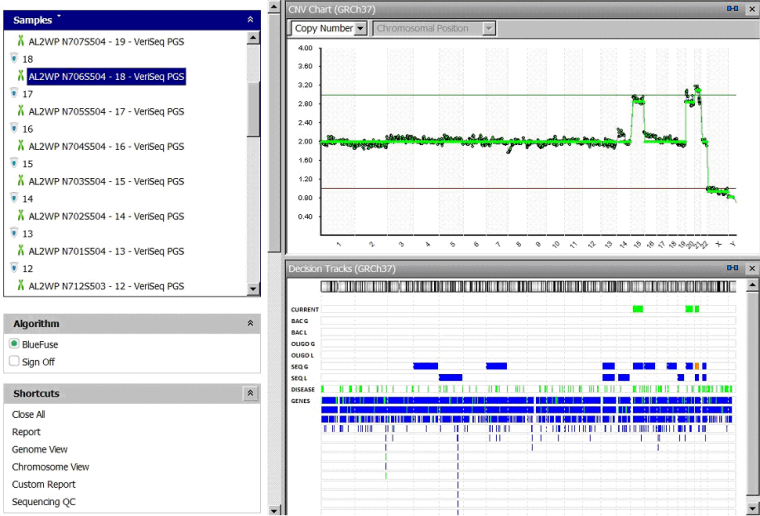
Рис. 1. Анеуплоидии у эмбриона по хромосомам 15, 20 и 21 у пациентки 40 лет методом NGS.
Что нам дает ПГД?
- Рождение здорового потомства;
- увеличение частоты имплантации;
- снижение частоты спонтанных абортов;
- снижение частоты многоплодных беременностей.
Фокус репродуктологов направлен на селекцию и перенос одного единственного здорового эмбриона в полость матки и получение беременности одним плодом, так как вынашивание многоплодной беременности зачастую связано с осложнениями во время беременности и преждевременными родами. Многие авторы делают заключение, что скрининг эмбрионов полезен для достижения этой цели.
Как проводится ПГД?
ПГД можно разделить на 2 этапа: 1- получение клеток от эмбрионов (работа проводится в лаборатории эмбриологии); 2 этап - собственно генетическое исследование полученного материала (проводится в лаборатории генетики). Забор клеток обычно производится на 5-6 сутки развития эмбриона (забирают от 2 до 6 клеток трофэктодермы). Для извлечения клеток производят насечку (хетчинг) на зоне пеллюцида эмбриона. Обычно эту процедуру проводят с помощью лазера, что практически не травматично для эмбрионов. Процедура занимает доли секунды. Полученные клетки передаются в лабораторию генетики для исследования, а эмбрионы продолжают культивировать или криоконсервируют для последующего переноса.
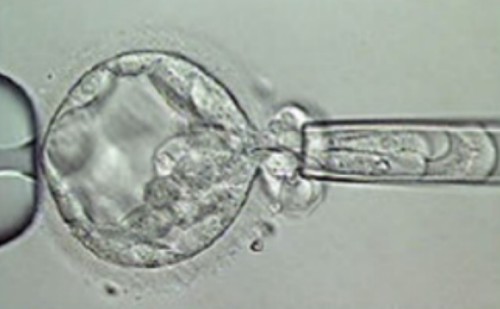
Рисунок 2. Биопсия клеток трофэктодермы у эмбриона 5 дня развития
Методы ПГД
Для генетического исследования большинство клиник применяют молекулярные (ПЦР) и молекулярно-цитогенетические методы (FISH и CGH).
- FISH (флуоресцентная гибридизация in situ) метод в последнее применяется очень редко. Это связано с его ограничениями: нет возможности проанализировать сразу все хромосомы, только определенное количество, а для успеха проведения программы ВРТ необходимо проанализировать как можно больше хромосом.
- Одним из распространенных генетических методов исследования является метод сравнительной геномной гибридизации (Comparative Genomic Hybridization — CGH). Данный метод позволяет осуществить исследование одновременно всех хромосом в эмбрионе (все 24 хромосомы) на предмет патологий.
- Применяя технику ПЦР, можно диагностировать заболевания, связанные с доминантными и рецессивными мутациями в уникальных генах (гемофилия, муковисцидоз и др.), определять антигены системы HLA, резус принадлежность эмбрионов, хромосомные нарушения (транслокации). Прежде чем проводить диагностирование у эмбрионов моногенных заболеваний, супружеская пара должна пройти подготовительный этап. В этом этапе в ряде случаев, помимо родителей, принимают участие и близкие родственники (зависит от конкретной ситуации). Необходимость в дополнительных исследованиях вызвана поиском так называемых маркеров около мутации. Этот этап необходим для более точного анализа нарушений у эмбриона.
- Самым инновационным методом в области ПГД является метод NGS (next generation sequencing, высокопроизводительное секвенирование). Принцип метода NGS принципиально отличается от других методов ПГС. Данный метод основан на определении последовательности ДНК, что открывает новые возможности в диагностике генетической патологии. Эта технология в последнее время все больше вытесняет метод CGH и находит более широкое применение в клиниках ВРТ за рубежом. Публикации разных авторов доказывают преимущества применения ее по сравнению с другими. Успех программы ЭКО после применения данного метода диагностики около 70%.
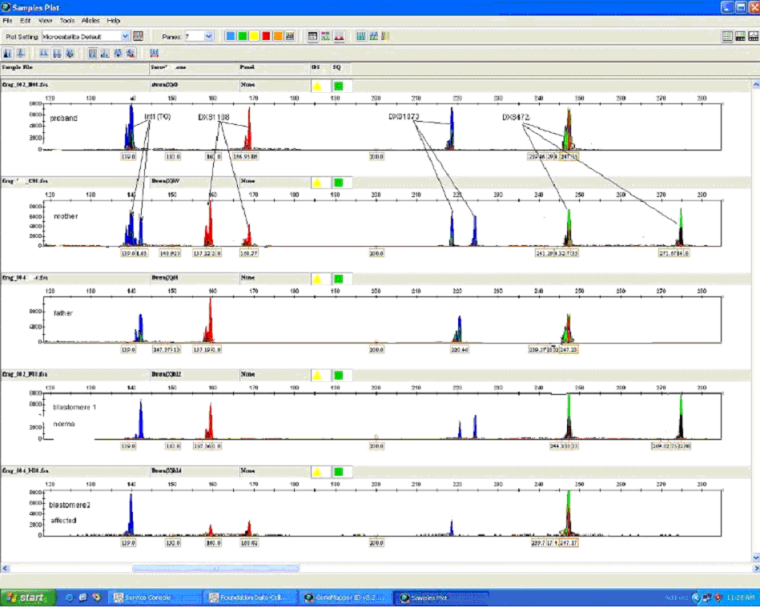
Рис.3. Генетическая диагностика у эмбрионов методом КФ-ПЦР.
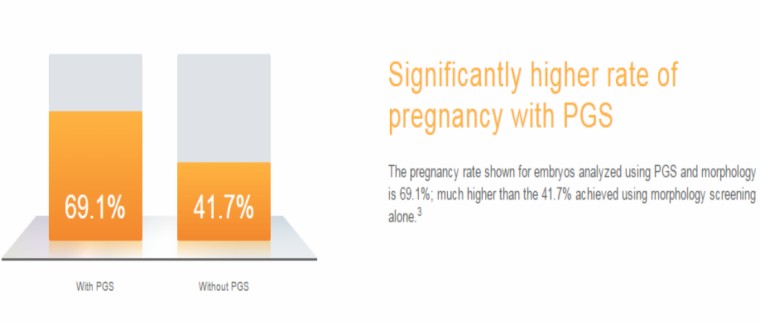
Рис. 4. Уровень наступления беременности в рамках программы ЭКО с проведением генетической диагностики и без.
Yang Z. с соавт. в своей работе рекомендует селективно переносить как можно меньше эмбрионов с учетом возраста, анамнеза и проведенных ранее циклов, при этом предварительно проводить ПГД. При переносе только одного эмбриона после ПГД беременность получена в 70.9% случаев.
Исследователи отметили высокий уровень имплантации эмбрионов у пациентов с ранее неудачными попытками ВРТ в анамнезе. Высокопроизводительное секвенирование (NGS), более четко указывает на наличие мозаицизма у преимплантационных эмбрионов, что позволяет выбрать генетически здоровые эмбрионы для переноса и повысить уровень наступления беременности.
Для сравнения приводим данные результатов, на изображении четко видны отличия (рис 5).
На верхних графиках представлены результаты анализа, полученные с помощью метода CGH, на нижних с помощью NGS.
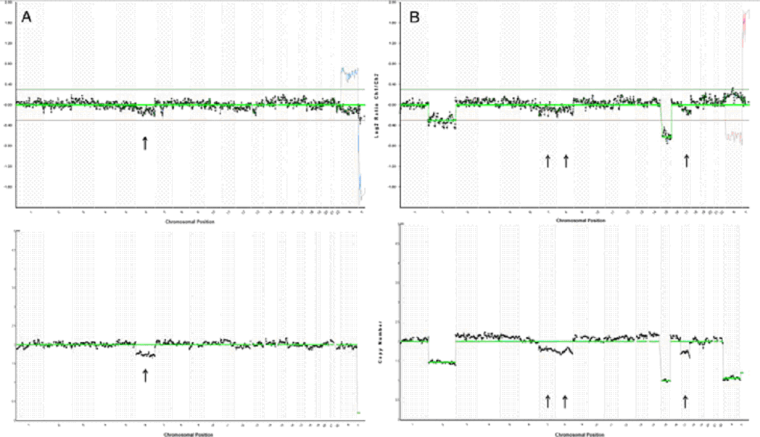
Рис.5. Результаты анализа, полученные с помощью метода CGH и NGS.
Еще несколько примером ПГД методом NGS
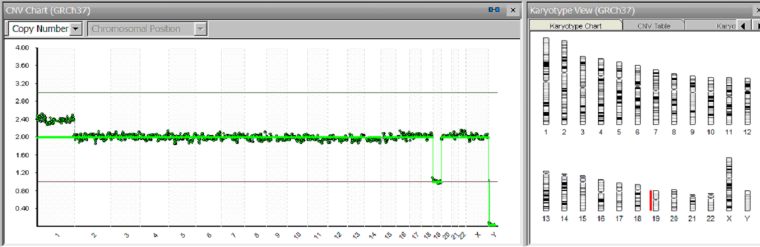
А)

В)
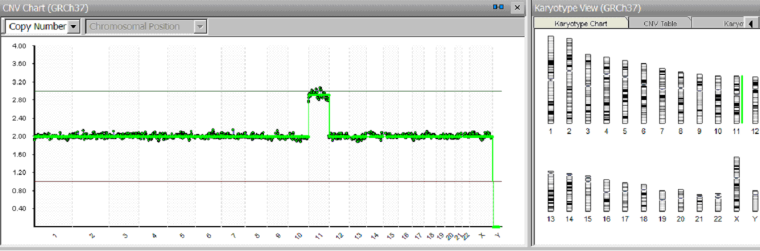
С)
Рисунок 6. Исследование клеток эмбрионов методом NGS.
А) в хромосомном наборе недостача хромосомы 19 (моносомия хромосомы 19) и мозаицизм хромосомы 1 (часть клеток содержит 2 хромосомы 1, а часть клеток содержит 3 хромосомы 1);
В) хромосомный набор эмбриона представлен множественными анеуплоидиями;
С) в хромосомном наборе присутствует лишняя хромосома 11 (трисомия хромосомы 11).
На какой стадии предпочтительно проводить ПГД?
Для проведения генетического анализа должна быть определенная концентрация ДНК. При работе с одной клеткой концентрация ДНК довольно низкая, поэтому предпочтительно для анализа иметь хотя бы несколько нитей ДНК (клеток). Следовательно, биопсия клеток трофэктодермы даст большее количество генетического материала и тем самым результат будет более достоверным и надежным.




